(Thethaovanhoa.vn) - Theo Chính phủ Mỹ và người đồng sáng lập công ty dược phẩm BioNTech, đơn đề nghị cấp phép sử dụng khẩn cấp vaccine ngừa COVID-19 do hai hãng dược phẩm Pfizer (Mỹ) và BioNTech (Đức) phối hợp phát triển sẽ được nộp lên Cơ quan quản lý thực phẩm và dược phẩm (FDA), Mỹ ngày 20/11. Bộ trưởng Y tế Mỹ Alex Azar đã xác nhận thông tin trên trong cuộc họp báo ngày 19/11 tại Washington.
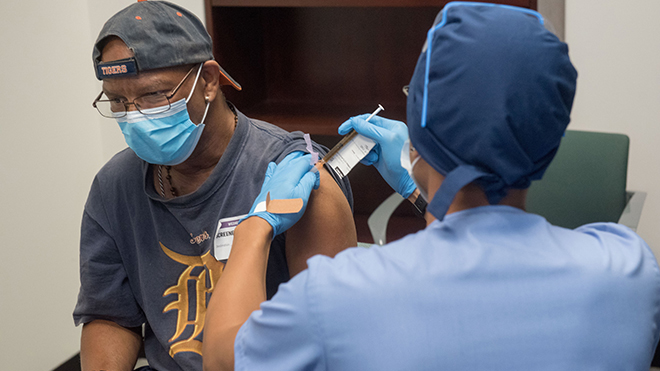
Tập đoàn công nghệ sinh học Moderna Inc của Mỹ ngày 16/11 thông báo vaccine thử nghiệm của hãng này đã phát huy tới 94,5% hiệu quả trong việc ngăn chặn virus SARS-CoV-2 gây bệnh viêm đường hô hấp cấp COVID-19
Trước đó, BioNTech thông báo hồ sơ xin cấp phép sẽ được hoàn tất trong ngày 19/11 và sẽ được nộp cho FDA. Việc xin cấp phép vaccine này chỉ mang tính ngắn hạn nhằm ứng phó với tình hình dịch bệnh khẩn cấp hiện nay, có thể được thu hồi hoặc điều chỉnh tùy thuộc hiệu quả và an toàn thực tế sử dụng sau đó.
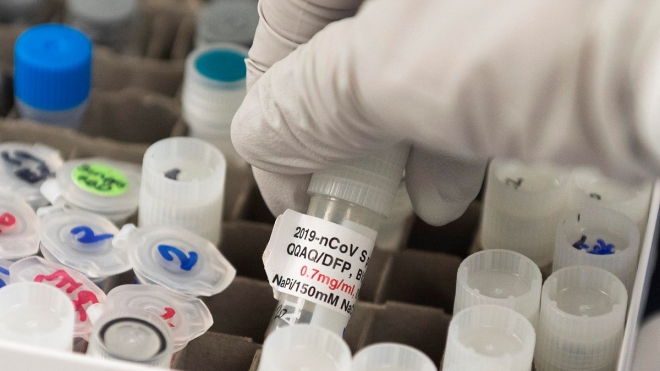 Vắcxin ngừa COVID-19 được phát triển bởi công ty Novavax tại Gaithersburg, bang Maryland, Mỹ. Ảnh: AFP/TTXVN
Vắcxin ngừa COVID-19 được phát triển bởi công ty Novavax tại Gaithersburg, bang Maryland, Mỹ. Ảnh: AFP/TTXVN
Hiện chưa rõ FDA sẽ xem xét hồ sơ trong bao lâu. Người đứng đầu cơ quan phát triển vaccine Mỹ Moncef Slaoui từng đề cập khả năng vaccine ngừa COVID-19 được "bật đèn xanh" cấp phép lưu hành vào tháng 12 tới - cùng thời gian nhà đồng sáng lập BioNTech Ugur Sahin dự kiến trước đó.
Ngày 18/11 vừa qua, Pfizer thông báo kết quả thử nghiệm cuối cùng loại vaccine ngừa COVID-19 do hãng cùng BioNTech phát triển cho thấy hiệu quả đến 95% và không có tác dụng phụ nghiêm trọng nào.
TTXVN